نريد اصناع إيثانوات الصوديوم في المخبر انطلاقاً من تفاعل إيثانوات الإيثيل مع محلول هيدروكسيد الصوديوم، عند درجة حرارة المحيط، هذا التحول تام و ينمذج بتفاعل كيميائي معادلته كما يلي:
معطيات:
- الناقلية المولية الشاردية عند لبعض الشوارد:
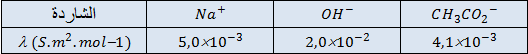
- الكتلة المولية لإيثانوات الإيثيل:
- الكتلة الحجمية لإيثانوات الإيثيل:
1- نضع في بيشر حجماً
1.1 - احسب كميات المادة الابتدائية في المزيج لكل من هيدروكسيد الصوديوم و إيثانوات الإيثيل
2.1 - أنشئ جدول تقدم التفاعل، وحدّد المتفاعل المحدّ.
2- نهمل الحجم
1.2- أكتب عبارة الناقلية النوعية للمزيج
2.2 - بين أن عبارة الناقلية النوعية للمزيج في اللحظة
3.2 - بين أن عبارة
3- متابعة الناقلية النوعية
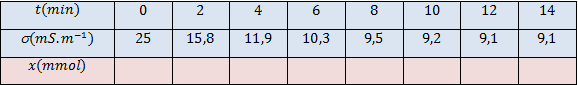
1.3 - لماذا تتناقص الناقلية النوعية للمحلول أثناء هذا التحوّل الكيميائي؟
2.3 - أكمل جدول القياسات بحساب قيم تقدم التفاعل
3.3 - عرّف السرعة الحجمية للتفاعل، كيف تتغير هذه السرعة بمرور الزمن؟ برّر إجابتك.
4.3- هل يمكن اعتبار التفاعل قد انتهى في اللحظة
5.3- عرّف زمن نصف التفاعل
6.3- نعيد نفس التجربة في حمّام مائي عند
1-1-
2.1 - جدول تقدم التفاعل:
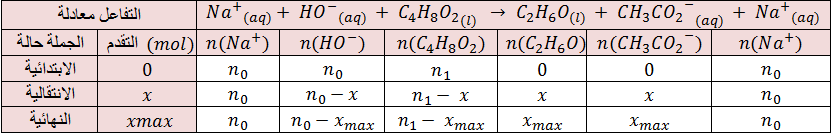
إذا كان
ومنه:
إذا كان
ومنه:
إذن:
والمتفاعل المحدّ هو: شوارد
1.2- عبارة
2.2 - عبارة
حيث:
ومنه:
3.2 - من جدول التقدم نجد:
بالتعويض فيعبارة
ومنه:
1.3 - تتناقص الناقلية النوعية للمحلول أثناء هذا التحوّل الكيميائي لأن ناقلية الشاردة الناتجة
2.3 - إكمال جدول القياسات ورسم المنحنى
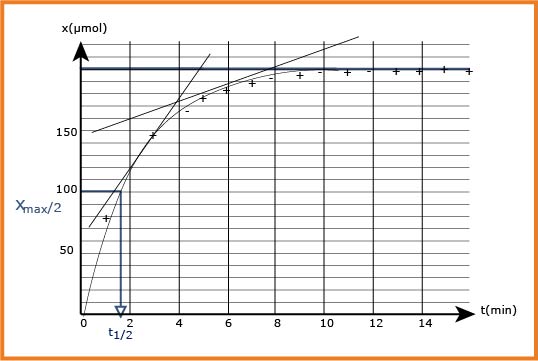
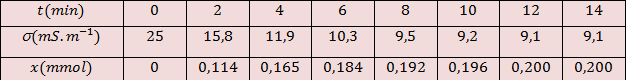
3.3 - السرعة الحجمية للتفاعل تعرّف بالعلاقة:
حيث:
هذه السرعة تتناقص بمرور الزمن لأنّ الميل يتناقص حتى ينعدم.
4.3-
5.3- زمن نصف التفاعل
بالاسقاط نجد:
6.3- رفع درجة الحرارة يسرّع التفاعل، فتنقص قيمة








