إن تفاعل كحول الايثانول
1- علما أن الثنائيتان الداخلتان في التفاعل هما:
بين أن معادلة التفاعل المنمذج للتحول الحادث هي:
ثم عين المُؤكسِد والمُرجِع.
2- في اللحظة

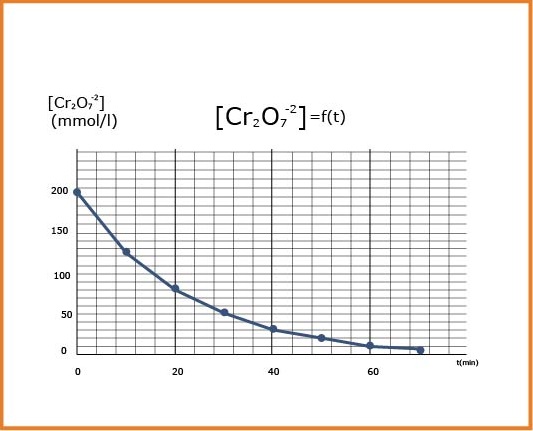
أ/ أرسم المنحنى البياني
ب/ أحسب كمية المادة الابتدائية للمتفاعلات. هل المزيج الابتدائي ستكيومتري ؟
جـ/ أنجز جدولا لتقدم التفاعل. ثم أحسب التقدم الأعظمي
3- عرف زمن نصف التفاعل
4- أ/ أعطي عبارة السرعة الحجمية للتفاعل بدلالة
أحسب قيمتها عند اللحظة
ب/ كيف تتطور قيمة السرعة الحجمية للتفاعل خلال الزمن؟ علل ثم فسر ذلك مجهريا
-1المعادلتين النصفيتين:
2 – أ- رسم المنحنى:
2 - ب:
-2 جـ حالة
حالة
-3 هو المدة الزمنية التي يبلغ فيها التفاعل نصف تقدمه النهائي
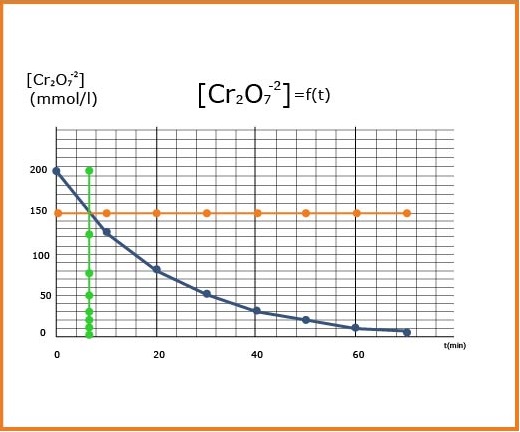
-4 أ
نرسم مماس المنحنى عند
4-ب- إن السرعة الحجمية للتفاعل تتناقص خلال الزمن لأن كميات المتفاعلات تتناقص حتى إحدى المتفاعلات تنتهي، عندئذا لا توجد إصطدامات فعالة








