أربعة محاليل مائية لها نفس التركيز المولي
- المحلول : محلول حمض الايثانويك
- المحلول : محلول غاز ميثان أمين
- المحلول : محلول ماءات البوتاسيوم
- المحلول : محلول حمض الآزوت
نقيس
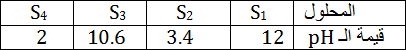
1 – حدث خلط لقيم الـ
2 – أكتب معادلتي تفاعل كل من حمض الايثانويك و غاز ميثان أمين مع الماء .
3 – أحسب النسبة النهائية لتقدم التفاعل
1-ترتيب قيم ال
المحلول
المحلول
المحلول
المحلول
2 – معادلات التفاعل:
- محلول حمض الايثانويك
- محلول غاز ميثان أمين
3 – النسبة النهائية لتقدم التفاعل :
نستنتج أن:حمض الايثانويك يتفكك جزئيا في الماء فهو حمض ضعيف يصل لحالة توازن أما حمض الآزوت فهو حمض قوي تفككه في الماءكلي ( تفاعل تام ).








