التمرين الأول :
أرادت مجموعتين من التلاميذ دراسة مدة اشتغال غواصة نووية يستهلك مفاعلها استطاعة قدرها
حيث
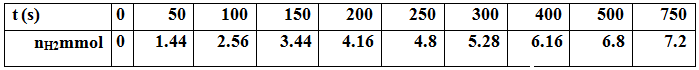
نلخص نتائج كل مجموعة في الجدول التالي:
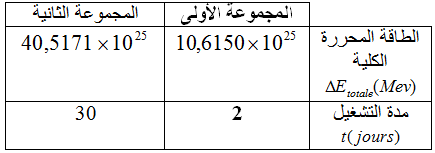
1/إن نظير لزركونيوم
أ- ماذا يمثل العددان
ب-ما معنى كلمة مشع ؟
ج-أكتب معادلة تفكك هذه النواة ؟
2/أحدى المجموعتين وصلت إلى نتائج صحيحة . لمعرفة من هي هذه المجموعة عليك بالإجابة على الأسئلة التالية:
أ-ما هو نوع التفاعل
ب-أحسب الطاقة المحررة بـ
ج-أحسب الطاقة المحررة لكتلة
د-على أي شكل تظهر هذه الطاقة ؟
ه-أحسب المدة الزمنية لاشتغال الغواصة
و-استنتج من هي المجموعة التي وصلت إلى النتائج الصحيحة ؟
المعطيات
التمرين الثاني
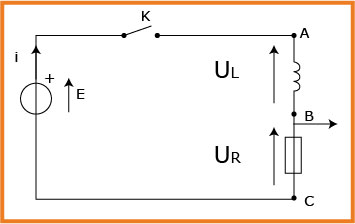
عند دراسة عملية شحن وتفريغ مكثفة يقوم تلميذ بتوصيلالعناصر الكهربائية كما هي مبينةفي الشكل المقابل حيث يضع القاطعة في الوضع
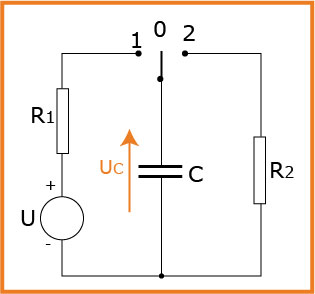
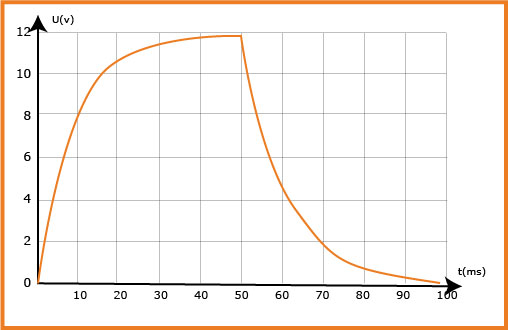
دراسة عملية الشحن:
1 - ما هو التوتر بين طرفي المكثفة عند نهاية الشحن ؟
2 - اكتب المعادلة التفاضلية التي يخضع لها التوتر بين طرفي المكثفة.
3- حل المعادلة من الشكل :
4 - أحسب قيمة سعة المكثفة إذا علمت أن
دراسة عملية التفريغ:
1- مثل دارة التفريغ وحدد جهة التيار
2- اكتب المعادلة التفاضلية التي يخضع لها التوتر بين طرفي المكثفة
3 - نضع
4 - احسب قيمة المقومة
التمرين الثالث:
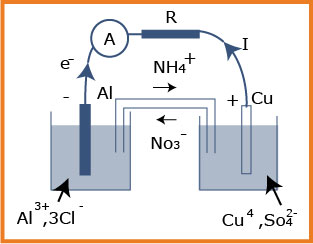
-Iنضع في بيشر حجما
في بيشر ثاني نضع حجما
نصل بين المحلولين بواسطة جسر ملحي يحتوي نترات الإمونيوم
عندما نصل بين الصفيحتين بواسطة مقياس فولط، حيث القطب السالب يتصل بصفيحة الألمنيوم، نقيس توترا
-1حدد قطبي العمود
-2ما هو دور الجسر الملحي؟
-IIنصل العمود بناقل أومي
-1أرسم شكلا تخطيطيا للعمود مع وضع البيانات، موضحا جهة التيار الكهربائي و جهة حركة مختلف حاملات الشحنة داخل و خارج العمود
-2أكتب معادلات التفاعل الحادث في كل مسرى مع تحديد إسمها و تحقق أن معادلة التفاعل تكتب:
-3ثابت التوازن الموافق لهاذا التفاعل هو:
أ-أحسب كسر التفاعل الإبتدائي
ب-بين إعتمادا على جهة التطور التلقائي لجملة أن جهة التطور لهذه الجملة يتوافق مع إشتعال العمود
-IIIيشتغل هذا العمود لمدة
-1أحسب كمية الكهرباء
-2أحسب كمية المادة من الإلكترونات
تعطى
التمرين الرابع
نعتبر قمرا اصطناعيا للاتصالالت كتلته
-1أعط تعريف المرجع المركزي الأرضي
-2ويجد القمر الاصطناعي على ارتفاع
-1-2أحسب
-2-2أعط مميزات شعاع السرعة المدارية
-3-2حدد مميزات شعاع التسارع
-3نعتبر المرجع المركزي الأرضي غاليليا نخضع القمر الاصطناعي في هذا المرجع إلى قوة وحيدة و هي قوة التجاذب التي تطبقها الأرض. نعتبر كتلة الأرض
-1-3بتطبيق القانون الثني لنيوتن، أوجد عبارة التسارع
-2-3أعظ عبارة السرعة المدارية
-3-3أعط عبارة الدور
-4-3استنتج عبارة القانان الثلث لكيبلر
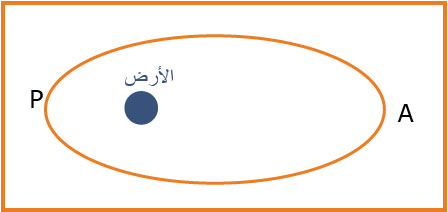
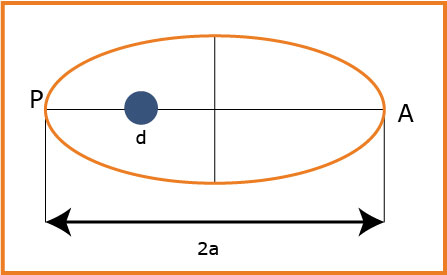
-4تتم عملية الإستقمار بواسطة صاروخ يقوم بحمل القمر الاصطناعي و وضعه في مدار انتظامي يكون شكل هذا المدار إهليليجي يمثل مركز الإرض إحدى محرقيه حيث الارتفاع الأصغري للقمر الاصطناعي هو
-1-4 في أي نقطة من المدار تكون سرعة القمر الاصطناعي أصغرية
-2-4 أعط عبارة الدور المداري
المعطيات:
التمرين الخامس :
الأمونياك ( النشادر )
1 – ما هو الأساس حسب برونشتد ؟
2 – أكتب معادلة انحلال هذا الغاز في الماء مبينا الثنائيتين : أساس / حمض الداخلتين في التفاعل .
3 – الناقلية النوعية لمحلول غاز نشادر تركيزه المولي
3 – 1- أكتب عبارة الناقلية النوعية لمحلول الأمونياك بدلالة التراكيز المولية للأفراد الكيميائية المتواجدة عند حالة التوازن والناقليات النوعية المولية للشوارد .
3 – 2- أحسب التركيز المولي النهائي للأفراد الكيميائية المتواجدة في محلول الأمونياك . ( نهمل التفكك الشارد للماء )
3 – 3- اكتب عبارة ثابت التوازن
3 – 4- أوجد العلاقة بين ثابت التوازن
4 – نحقق معايرة
4 – 1- أكتب المعادلة الكيميائية المنمذجة للتفاعل الحادث .
4 – 2- ما هو الحجم اللازم إضافته من محلول حمض كلور الماء حتى يحدث التكافؤ ؟
4 – 3- بيّن أنه عند إضافة
يعطى :
التمرين التجريبي :
أراد أحد التلاميذ دراسة التحول الكيميائي الذي يحدث للجملة ( محلول حمض كلور الهيدروجين ، الزنك ) و الذي ينمذج بتفاعل كيميائي معادلته :
في اللحظة
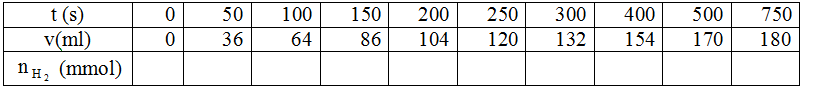
1) أحسب في كل لحظة
2) أحسب كميات المادة الإبتدائية للمتفاعلات .
3) أنجز جدولا لتقدم التفاعل واستنتج العلاقة بين التقدم
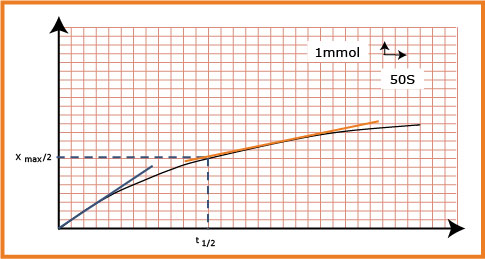
4) أرسم البيان
5) ما هي قيمة السرعة الحجمية للتفاعل في اللحظات
6) إذا كان التفاعل تاما فأوجد :
أ ـ المتفاعل المحد.
ب ـ التقدم الأعظمي
ج ـ زمن نصف التفاعل
تعطى :
التمرين الأول :
1-أ- العدد
ب- نظير مشع أي أنه يتفكك تلقائيا مصدرا إشعاعات (غير مستقر (
ج- معادلة تفكك هذه النواة
مبدأ انحفاظ الكتلة
مبدأ انحفاظ الشحنة
اي
2- أ – نوع التفاعل
ب- الطاقة المحررة
ج- الطاقة الناتجة عن انشطار هذه الكتلة هي
عدد الأنوية الموجود في هذه الكتلة هي
د- تظهر هذه الطاقة على شكل طاقة حركية لمكونات
هـ- المدة الزمنية لإشتغال الغواصة : لدينا استطاعة التحويل
و- المجموعة التي وصلت إلى نتائج صحيحة هي المجموعة الثانية بمقامة نتائج متوصل إليها مع نتائج المدونة في الجدول
التمرين الثاني
دراسة عملية الشحن
1- التوتر بين طرفي المكثفة عند نهاية الشحن
2- حسب قانون التوترات :
3-حل المعادلة من الشكل :
وباشتقاق العبارة السابقة تتحصل على :
وبتعويض في المعادلة التفاضلية نجد أنه لتقبل بأن يكون حلا يجب أن يكون
ثابت الزمن
4- قيمة سعة المكثفة :
دراسة عملية التفريغ
1- تمثيل الدارة و تحديد جهة التيار
2- المعادلة التفاضلية التي يخضع لها التوتر بين طرفي المكثفة
3-تحقق من أن
وباشتقاق نجد أن
نعم تقبل حلا
4- قيمة المقومة
التمرين الثالث:
- مسرى النحاس يمثل القطب
- مسرى الالمنيوم يمثل القطب
-2 الجسر الملحي وسمح بمرير التيار و يحافظ على التوازن الكهربائي للمحلولين
-1-II
-2 عند القطب
عند القطب
و لنحقق:عدد الالكترونات المفقودة خلال الأكسدة يساوي عدد الالكترونات المكتسبة خلال الارجاع. لدينا بجمد المعادلتين:
-3 أ-
ب
III-
1-
2-
التمرين الرابع
-1المرجع المركزي الأرضي:يستعمل لدراسة حركة الأجسام حول الأرض مبدأ هذا المعلم موجود في مركز الأرض
1-2-
-2-2شعاع السرعة
-3-2شعاع التسارع
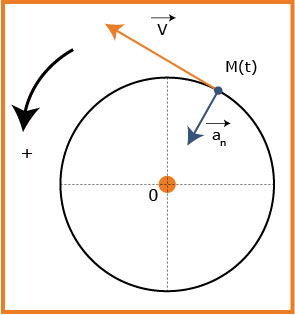
-1-3بتطبيق قانون نيوتن الثاني:
شدتها حسب المحور الموجه
$$a_n=\frac{GM_T}{r^2}=\frac{v^2}{r}
و منه
3-3-
-4-3عبارة القانون الثلث لكيبلر:
بتربيع الطرفين:
بوضع
-1-4تكون سرعة القمر الإصطناعي ـاصغرية عند النقطة
-نحسب المسافة بين مركز الأرض و النقطة :
التمرين الخامس
-1 الأساس هو كل فرد كيميائي قادر على التقاط بروتون
2- الثنائيتين أساس/ حمض :
1-3- الناقلية النوعية للمحلول عند حالة التوازن :
2-3بإهمال التفكك الشاردي للماء :
3 – 3 : اكتب عبارة ثابت التوازن
3 – 4 ثابت الحموضة
4 – 1 : أكتب المعادلة الكيميائية المنمذجة للتفاعل الحادث
4 – 2 الحجم اللازم إضافته من محلول حمض كلور الماء حتى يحدث التكافؤ
عند التكافؤ :
4 – 3 : عند اضافة حجم :
نحصل على نقطة نصف التكافؤ و عندها :
التمرين التجريبي :
1- حساب في كل لحظة
لدينا
2-حساب كميات المادة الإبتدائية للمتفاعلات :
3- انجاز جدول لتقدم التفاعل واستنتاج العلاقة بين التقدم
ـ جدول تقدم التفاعل
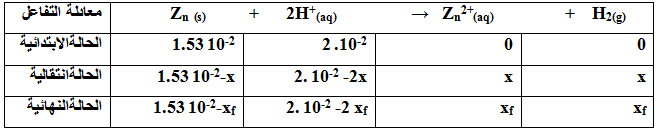
ـ العلاقة بين التقدم
4- رسم البيان
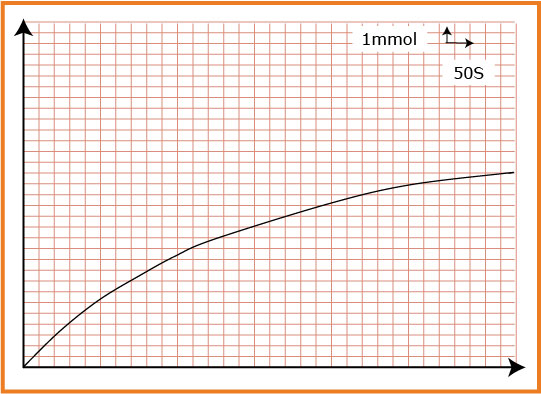
6) السرعة الحجمية للتفاعل :
حيث
نلاحظ أن السرعة الحجمية للتفاعل تناقصت وذلك لتناقص تركيز المتفاعلات
6- إذا كان التفاعل تاما
أو
وقيمة
إذا المتفاعل المحد هو شوارد
ــ زمن نصف التفاعل فهو الزمن الموافق ل :
و من المنحنى نجده حوالي :
لرسم للتوضيح فقط .