نذيب حمض الميثانويك
قياس ال
1-1 - أكتب معادلة التفاعل الكيميائي الحادث.
1-2- انشأ جدول التقدم واستنتج المتفاعل المحد.
1-3- احسب التقدم النهائي
1-4- استنتج نسبة التقدم النهائي
2- نمزج حجم
قياس
2-1- كيف تغير
2-2- اكتب معادلة التفاعل حمض – اساس الحادث.
2-3- انشأ جدول تقدم التفاعل بدلالة التقدم
2-4- عين التقدم الأعظمي و نسبة التقدم النهائي . ماذا تستنتج ؟
1-1-معادلة التفاعل بين حمض الميثانويك و الماء:
1-2- جدول تقدم التفاعل :
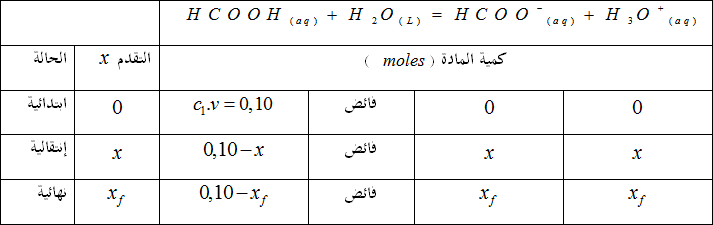
يتواجد الماء في المحلول الحمضي بكميةة فائضة: فان المتفاعل المحد هو حمض الميثانويك.
1 -3- حساب التقدم النهائي : حسب الحالة النهائية للجملة الكيميائية :
حساب التقدة الأعظمي : من جدول التقدم :
4-1- نسبة التقدم النهائي :
فالتحول الكيميائي ليس تاما.
1-2- ان الــــــ
و ذلك لسبب تفاعلها مع شوارد الميثانوات
2-2- معادلة التفاعل حمض – أساس الحادث في المزيج :
3-2- جدول تقدم التفاعل :
أ) -
ب)-
منه :

-4- حساب التقدم الأعظمي :
مع :
فان المتفاعل المحد هو شاردة الأوكسونيوم
نسبة التقدم النهائي : في الحالة النهائية للمزيج :
و
بالمطابقة :
فان :








