نعتبر العمود ذي الرمز
1/ حدّد الثنائيتين :
الثنائيتين
2/ أكتب المعادلتين النصفيتين عند المسريين، ثم معادلة التفاعل المنمذج للتحول الكيميائي الذي يحدث في العمود .
أكسدة
إرجاع
معادلة التفاعل المنمذج للتحول الكيميائي الذي يحدث في العمود:
3 ـ1/ أحسب الكسر الابتدائي للتفاعل، و مذا تستنتج؟.
الكسر الابتدائي للتفاعل:
نستنتج أن التفاعل تام
3 ـ2/ إذا كان ثابت التوازن الموافق للتفاعل السابق في الاتجاه المباشرهو
4/ إذا كان العمود ينتج تياراً كهربائياً مستمراً شدته
4 ـ1/ أحسب كمية الكهرباء التي ينتجها العمود خلال هذه المدة.
نعلم أن قانون كمية الكهرباء هو:
4 ـ 2 /عيّن التركيز المولي لكل من
جدول تقدم التفاعل
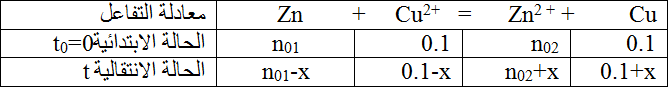
من معادلة التفاعل:
و منه:
لكن:
فأخيرا:
تركيز
تركيز








